存在的挑战
JAK/TYK激酶是多种炎症性疾病中的关键信号分子。以银屑病为例,炎症反应由干扰素和细胞因子释放增加驱动,而这一过程受JAK/TYK激酶调控。
目前已上市药物均以这些多结构域蛋白复合物的JH1激酶结构域为靶点,但这类获批的JAK抑制剂因对其他JAK激酶(JAK1、JAK2、JAK3)存在非选择性抑制,已知会引发与心脏功能、凝血及血栓相关的安全性问题。
因此,Nimbus Therapeutics的科学家们着手应对这一挑战,旨在开发一种强效、高选择性的TYK2抑制剂,以提升临床疗效并避免脱靶副作用。
TYK2是白细胞介素12(IL-12)、白细胞介素23(IL-23)及Ⅰ型干扰素信号通路的关键介导分子,这些细胞因子与多种炎症性疾病及自身免疫性疾病的发病机制相关,例如银屑病、类风湿关节炎、狼疮及炎症性肠病等。
在人类全基因组关联研究的有力数据及临床结果支持下,通过小分子药物抑制TYK2活性已成为治疗此类疾病的一种极具吸引力的治疗策略。
2016年,Nimbus与Schrödinger(薛定谔)的科学家团队展开合作,初期以催化JH1激酶结构域为靶点,后续基于文献中发布的突破性数据,转向调控结构域JH2的研究。
首次将大规模自由能微扰(FEP+)技术应用于药物研发
首次通过FEP+技术发现新型皮摩尔级核心结构
应用创新性基于物理的溶解度预测方法
“我们的团队借助下一代基于物理的技术对先导化合物进行设计、迭代与优化,这使我们能够快速完善研发方法。此次合作不仅为Nimbus提供了无与伦比的计算能力,更取得了前所未有的FEP+建模成果。”
—— Craig Masse
Nimbus Therapeutics前药物化学负责人
靶向TYK2 JH1催化结构域:借助大规模FEP+技术实现TYK2选择性与溶解度的突破
JAK家族中TYK2的高序列相似性构成了重大的选择性挑战,TYK2、JAK1、JAK2和JAK3的配体结合位点几乎完全一致。为设计出兼具活性与低脱靶风险的高选择性、强效分子,团队通过大规模基于物理的模拟来区分激酶间的结合差异。
首先,利用FEP+进行自由能微扰计算,预测对TYK2靶点的效力以及对JAK2和JAK3脱靶靶点的效力;随后,团队引入一种基于绝对FEP+的新型水溶性预测方法,以便在建模过程中解决药物代谢动力学(ADME)特性相关问题。
下一个关键步骤是开展大规模FEP+评分研究,以应对多参数优化(MPO)挑战。团队凭借深厚的药物化学知识和建模专业能力,筛选出4000个高质量候选分子,所有分子均通过了MM-GBSA(分子力学-广义玻恩表面积)和物理性质过滤器的初步筛选。
随后,通过FEP+对这些分子的效力、选择性和溶解度进行评分(如下图)。要实现如此大规模的FEP+评分应用,需将FEP+部署到大规模云计算资源中,这一方法自首次应用后已成为行业的常用手段。
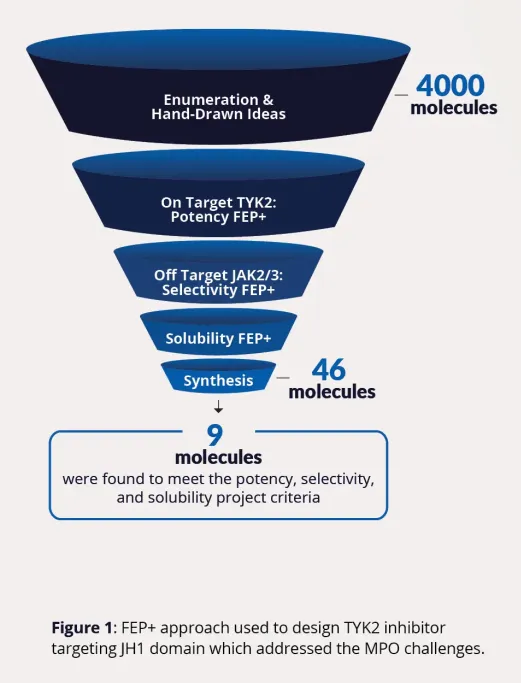
图注:用于设计靶向JH1结构域TYK2抑制剂的FEP+方法
最终,根据FEP+计算结果,优先合成了46个分子,其中9个分子在后续实验测试中满足效力、选择性和溶解度的要求。这些成果催生了针对TYK2 JH1结构域的候选药物,它对JAK2具有高选择性,对JAK1和JAK3具有中等选择性。
针对TYK2 JH1结构域的化合物能否进入临床试验呢?敬请关注下一篇。



